это один из самых легких металлов
Литий⁚ легкий металл с широким спектром применения
Литий – это химический элемент, относящийся к щелочным металлам. Он имеет атомный номер 3 и обозначается символом Li. Литий ⏤ это один из самых легких металлов, он мягкий, серебристо-белый и легко поддается механической обработке.
Литий – это химический элемент, относящийся к щелочным металлам. Он имеет атомный номер 3 и обозначается символом Li. Литий ⎼ это один из самых легких металлов, он мягкий, серебристо-белый и легко поддается механической обработке. В природе литий встречается в виде соединений, а не в чистом виде, и его добыча представляет собой сложный процесс, требующий специальных технологий.
Литий был открыт в 1817 году шведским химиком Йоханом Августом Арфведсоном, который обнаружил его в минерале петалите. В 1855 году британский химик Роберт Бунзен и немецкий физик Густав Кирхгоф разработали метод получения лития в чистом виде, используя электролиз его хлорида.
Литий – это редкий металл, но он встречается в небольших количествах во многих минералах, таких как сподумен, лепидолит и амблигонит. Основными производителями лития являются Австралия, Чили, Китай и Аргентина.
Литий играет важную роль в различных областях науки и техники. Его используют в производстве аккумуляторов, керамики, стекла, смазочных материалов, а также в ядерной энергетике. Благодаря своим уникальным свойствам, литий становится все более востребованным материалом в современном мире.
2. Свойства лития⁚
Литий обладает уникальным набором физических и химических свойств, которые делают его ценным материалом для различных применений.
Физические свойства лития включают⁚
- Низкую плотность⁚ Литий ⏤ это самый легкий металл, его плотность составляет всего 0,534 г/см³. Это делает его идеальным материалом для использования в легких сплавах и аккумуляторах.
- Низкую температуру плавления⁚ Литий плавится при температуре 180,54 °C, что делает его легкоплавким металлом.
- Высокую теплоемкость⁚ Литий обладает высокой теплоемкостью, что означает, что он может поглощать значительное количество тепла без существенного повышения температуры.
- Хорошую электропроводность⁚ Литий является хорошим проводником электричества, что делает его ценным материалом для использования в электрохимических устройствах, таких как аккумуляторы.
Химические свойства лития включают⁚
- Высокую реакционную способность⁚ Литий очень реакционноспособен и легко вступает в химические реакции с водой, кислородом и другими веществами.
- Образование стабильных соединений⁚ Литий образует стабильные соединения с различными элементами, такими как галогены, кислород и азот.
- Высокую электроотрицательность⁚ Литий обладает высокой электроотрицательностью, что означает, что он легко отдает электроны и образует катионы.
Важно отметить, что литий является очень активным металлом и требует осторожного обращения. При работе с литием необходимо соблюдать меры предосторожности, чтобы избежать пожаров и взрывов.
2.1. Физические свойства
Литий обладает уникальным набором физических свойств, которые делают его ценным материалом для различных применений.
Низкая плотность является ключевой особенностью лития. Он ⏤ самый легкий металл, его плотность составляет всего 0,534 г/см³. Это делает его идеальным материалом для использования в легких сплавах, которые применяются в авиационной и космической промышленности, а также в производстве спортивного инвентаря.
Низкая температура плавления лития (180,54 °C) делает его легкоплавким металлом. Это свойство важно при производстве литиевых аккумуляторов, где литий используется в виде электролита.
Высокая теплоемкость ⏤ еще одно важное свойство лития. Это означает, что он может поглощать значительное количество тепла без существенного повышения температуры. Это свойство делает литий ценным материалом для использования в системах теплопередачи и в качестве теплоносителя.
Хорошая электропроводность лития делает его ценным материалом для использования в электрохимических устройствах, таких как аккумуляторы. Литий-ионные аккумуляторы, которые широко используются в мобильных устройствах, электромобилях и других устройствах, работают на основе ионов лития, которые перемещаются между электродами.
2.2. Химические свойства
Литий – это активный металл, который легко вступает в химические реакции. Он обладает высокой реакционной способностью, особенно с водой и кислотами.
Реакция с водой⁚ Литий бурно реагирует с водой, образуя гидроксид лития (LiOH) и водород (H₂). Эта реакция экзотермическая, то есть выделяет тепло.
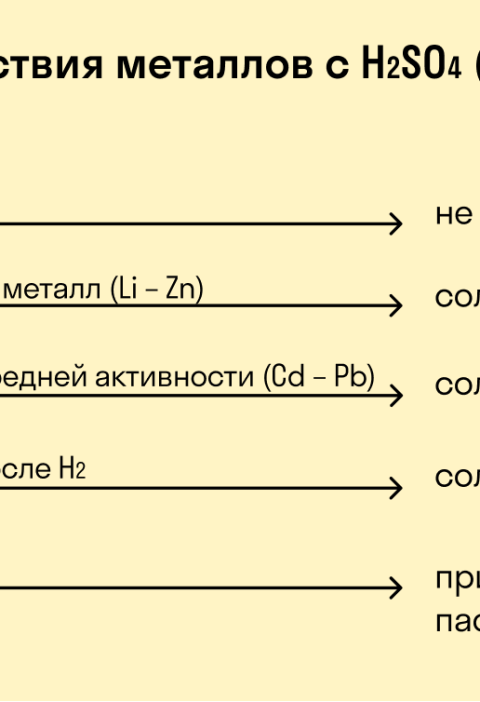
Реакция с кислотами⁚ Литий реагирует с кислотами, такими как соляная кислота (HCl) и серная кислота (H₂SO₄), с выделением водорода.
Образование солей⁚ Литий образует соли с различными анионами, такими как хлорид (Cl⁻), сульфат (SO₄²⁻) и карбонат (CO₃²⁻). Эти соли широко используются в различных отраслях промышленности.
Реакция с кислородом⁚ Литий легко реагирует с кислородом, образуя оксид лития (Li₂O). Эта реакция происходит при комнатной температуре, поэтому литий необходимо хранить в инертной атмосфере.
Реакция с азотом⁚ При высокой температуре литий реагирует с азотом, образуя нитрид лития (Li₃N).
Реакция с галогенами⁚ Литий реагирует с галогенами, такими как хлор (Cl₂), бром (Br₂) и йод (I₂), образуя галогениды лития.
Реакция с органическими соединениями⁚ Литий также может вступать в реакции с органическими соединениями, образуя различные литийорганические соединения, которые используются в органическом синтезе.